衰老是我们每个人都需要面对的现象,它所带来的影响体现在我们身体的方方面面,其中便包含了机体免疫系统的衰老。衰老后的免疫系统一方面难以识别体内细胞或分子的细微变化,出现免疫“漏洞”,导致老年人恶性肿瘤的发病率高于年轻时;另一方面其对外界刺激的反应能力下降,无法有效抵御病原体的入侵,这意味着老年人容易发生细菌、病毒或真菌等病原体感染性疾病,接种疫苗的效果往往也显著低于年轻人。此外,老年人体内慢性炎症的水平往往也更高,这是由于衰老的免疫系统更倾向于激发炎症反应,而不是清除炎症反应。这种高炎症水平的现象不仅损害了正常组织,还可能促进了多种与年龄相关的疾病的发展。
2023 年一篇纳入了 43096 名参与者(年龄分布 20-88 岁)的中国成年人免疫系统与衰老研究发现,在 35 岁以后,中国成年人体内的免疫系统就逐渐开始走“下坡路”[1]。为了能够有效缓解衰老的进程,人们提出了许多种方法,如保持固定的生活作息、采用营养均衡的膳食和保持健康的锻炼等良好生活习惯,或者通过正念禅修和针灸等方式,不可否认这些方法的确都起到了一定的作用。然而,衰老依旧像是车轮一般滚滚向前,我们能否找到某种方式将这个“车轮”停下,甚至是逆转呢?
近日,来自斯坦福大学的Irving L. Weissman 研究团队和美国国立卫生研究Kim J. Hasenkrug团队合作在Nature期刊上发表了题为Depleting myeloid-biased haematopoietic stem cells rejuvenates aged immunity的研究论文[2],研究团队开发了一种抗体疗法,能够靶向清除小鼠体内的髓系偏向造血干细胞,使得老年小鼠恢复了年轻时免疫系统的特征,包括增加淋巴细胞祖细胞、新生 T 细胞和 B 细胞数量,同时减少了衰老免疫系统的相关标志物的表达。并且这种抗体疗法增加了老年小鼠对于病毒感染的免疫反应,使得疫苗接种效果得到了提高。

造血干细胞(haematopoietic stem cells,HSCs)是作为人体内一种至关重要的细胞类型,驻扎在骨髓内,担负着生成血液细胞保障生理功能,以及生虫各种免疫细胞如 T 细胞、B 细胞和自然杀伤细胞等的重任。同时,造血干细胞具有强大的自我更新能力,能够通过分裂产生与自己相同的干细胞,维持自身数量的稳定,让机体即使在面临外部压力或内部损伤时,也能迅速恢复和适应。通常,造血干细胞可以分为两类:淋巴-髓系平衡造血干细胞(HSCs with balanced output of lymphoid and myeloid cells,bal-HSCs)和髓系偏向造血干细胞(HSCs with myeloid-biased output,my-HSCs)。随着年龄的增加,造血干细胞的主要类型会从 bal-HSCs 逐渐变化为 my-HSCs,从而减少了淋巴细胞的生成,增加了髓系细胞的生成。后者也正是众多老年问题——免疫衰退,慢性炎症,甚至是髓系相关疾病产生的元凶。理论上,如果能够清除 my-HSCs,是有可能使得体内 bal-HSCs 含量重新变多从而恢复免疫系统的“年轻”。
为了达到这一目的,研究团队首先要找到特异性表达在 my-HSCs 上的抗原,从而设计针对性抗体清除 my-HSCs。通过组学分析和流式细胞术,研究团队发现相比于 bal-HSCs,在 my-HSCs 中,CD62p 和 NEO1 这 2 个基因具有最高的表达量(图1)。基于 CD62p、NEO1 和 CD150(已知区分 my-HSCs 和 bal-HSCs 的标志物)三者,研究团队能够很好地将 my-HSCs 从其它造血干细胞中区分出来。研究团队分别设计了针对这三个抗原的特异性抗体 anti-CD62p、anti-NEO1 和 anti-CD150,发现任意一种抗体都能减少动物体内 my-HSCs 的数量,但由于每个细胞表面分布的抗原蛋白并不完全一样,因此只针对单个抗原蛋白的清除 my-HSCs 效果并不佳。在经过优化后,研究团队将任意一种抗体与 anti-CD47 和 anti-KIT(这两者与抗巨噬细胞吞噬相关,会在病变或衰老机体内异常活跃)联用,发现能够显著提高 my-HSCs 的清除效率。
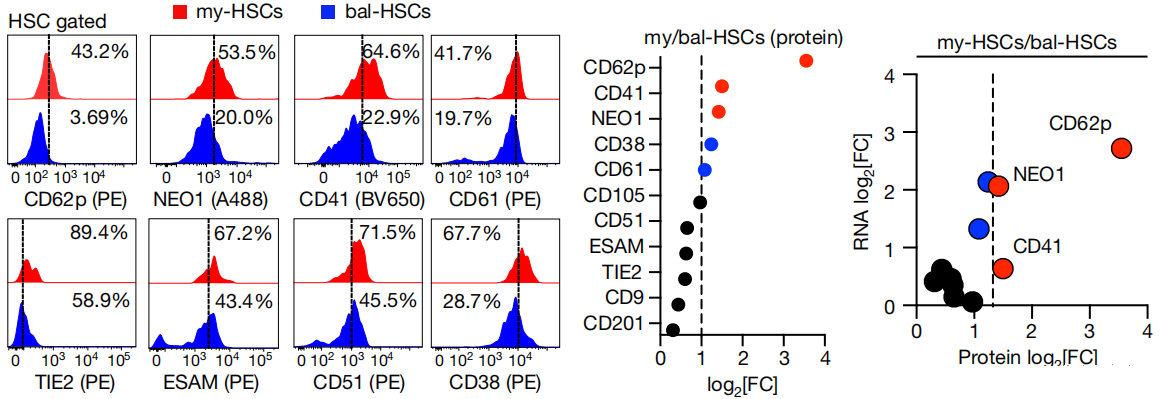
图1 鉴别和验证my-HSCs表面抗原的流程示意图,及bal-HSCs与my-HSCs细胞表面抗原含量。
随后研究团队在衰老小鼠上使用了这些抗体疗法(图2)。他们发现衰老小鼠在注射第一周后就出现了明显的 my-HSCs 数量下降,并且这种下降趋势在随后的治疗过程中得到了进一步巩固和提高。相对应的,bal-HSCs 及其子代细胞的数量也都出现了显著的增加,而这些细胞正是免疫系统“年轻”的关键。这些数据进一步证实了研究团队设计的抗体疗法的强大潜力与真实性。得益于生力军的补充,注射抗体疗法后的衰老小鼠的淋巴细胞衰老相关的免疫表型也得到了抑制,对于感染的抵抗力和疫苗的接种效果也都得到了显著的改善。同时,衰老小鼠体内慢性炎症相关的炎症因子水平也出现了下降。
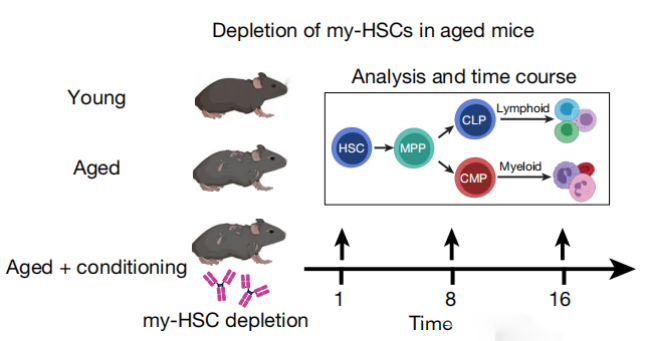
图2 在治疗 1、8 和 16 周后比较年轻小鼠和衰老小鼠体内免疫系统状况
更令人振奋的是,研究团队在分析了人类造血干细胞表面抗原的表达情况后,发现人类造血干细胞中 CD62p 和 NEO1 在 my-HSCs 中表达量也升高了,并且能够被同样的抗体识别和筛选。这种不同物种间的保守性表明,这项临床前研究可以向临床治疗方案转化,以帮助人类免疫系统恢复年轻状态。
同期Nature上也刊登了知名干细胞学者 Robert A. J. Signer 教授的评论文章“Anti-ageing antibodies revive the immune system”。Signer 教授在称赞该抗体疗法的同时也指出了其可能存在的潜在风险,如抗体注射可能会缩小造血干细胞的总量,从而加剧克隆性造血的出现,也可能迫使造血干细胞出现代偿性地扩张,这就可能会导致相关癌症的发生,警醒人们在未来转化此种抗体疗法时应当注意不能过度使用。
研究的第一作者 Jason B. Ross 说:“这是一个真正的思想范式转变——研究人员和临床医生应该以一种新的方式来思考免疫系统和衰老。仅仅通过影响如此少量细胞的功能,就有可能调整整个免疫系统,这一想法令人惊讶和兴奋。”
无论如何,这一研究不仅开启了一条通过靶向特定细胞以重振免疫系统和缓解衰老影响的新途径,还为我们提供了抵抗衰老的希望。通过这种创新的抗体治疗,我们或许能够迈向一个更健康长寿的未来。
参考文献:
[1] Jia Z, Ren Z, Ye D, et al. Immune-Ageing Evaluation of Peripheral T and NK Lymphocyte Subsets in Chinese Healthy Adults.Phenomics. 2023;3(4):360-374. Published 2023 May 23. doi:10.1007/s43657-023-00106-0
[2] Ross JB, Myers LM, Noh JJ, et al. Depleting myeloid-biased haematopoietic stem cells rejuvenates aged immunity.Nature. 2024;628(8006):162-170. doi:10.1038/s41586-024-07238-x